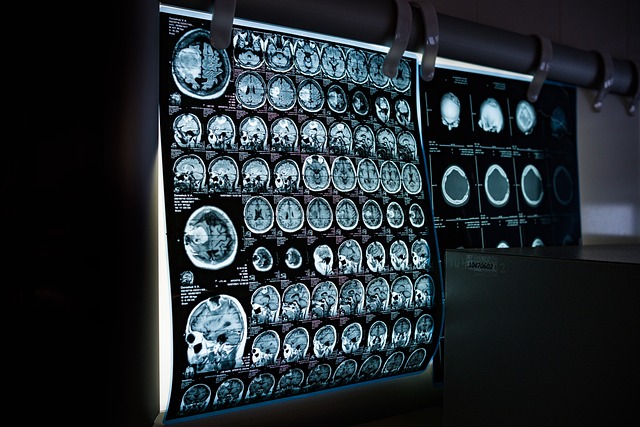
Opzioni terapeutiche aggiornate per la salute della prostata
La gestione del tumore prostatico si basa su una valutazione individuale che integra diagnosi, stadiazione e preferenze del paziente. Le opzioni terapeutiche variano da strategie di sorveglianza a interventi locali e terapie sistemiche, con crescente attenzione a genetica e biomarker per personalizzare le scelte.
La diagnosi precoce e la scelta di un percorso terapeutico appropriato sono fondamentali per la salute della prostata. Il trattamento contempla molteplici discipline, tra cui urologia e oncology, e combina approcci locali e sistemici in base allo stadio, all’età e alle condizioni generali del paziente. Decisioni informate richiedono informazioni da biopsia, imaging e, sempre più spesso, da test genetici e biomarcatori per distinguere malattie indolenti da forme aggressive.
Questo articolo è solo a scopo informativo e non deve essere considerato un consiglio medico. Consultare un professionista sanitario qualificato per indicazioni e trattamenti personalizzati.
Urologia e oncologia: quali ruoli?
Urologia e oncology collaborano strettamente nella gestione del tumore prostatico. L’urologo è spesso il primo specialista coinvolto per visita clinica, ecografia e indicazione alla biopsia; l’oncologo è centrale quando sono necessarie terapie sistemiche come chemotherapy o immunotherapy. La scelta del percorso terapeutico dipende dalla stadiazione TNM, dal punteggio Gleason/ISUP e dalla presenza di metastasis. Nei casi a basso rischio, la sorveglianza attiva è gestita con controlli periodici tra team multidisciplinari. È importante che il paziente abbia accesso a local services competenti e che le decisioni siano condivise tra specialisti.
Diagnosi: biopsia e imaging
La biopsia rimane la conferma diagnostica fondamentale; negli ultimi anni si è diffuso l’uso di imaging avanzato come la risonanza magnetica multiparametrica (mpMRI) per guidare la biopsia mirata e migliorare la rilevazione delle lesioni clinicamente rilevanti. Procedure di biopsia possono essere eseguite per via transrettale o transperineale, con diverse implicazioni di rischio di infezione. L’imaging è anche cruciale per la stadiazione e il monitoraggio della sorveglianza attiva: ecografia, TC e PET/CT con traccianti specifici supportano la valutazione di metastasis e la pianificazione terapeutica.
Terapie locali: surgery e brachytherapy
Le opzioni locali comprendono chirurgie (prostatectomia radicale) e tecniche di radiation come la brachytherapy o la radioterapia esterna. La scelta tra surgery e radioterapia dipende da fattori come età, aspettativa di vita, preferenze personali e comorbilità. La brachytherapy, con impianto di sorgenti radioattive direttamente nella ghiandola, è indicata in pazienti selezionati con malattia a rischio intermedio-basso e tende a ridurre l’irradiazione dei tessuti circostanti. La chirurgia offre l’asportazione completa dell’organo e informazioni istologiche dettagliate, ma comporta rischi urologici e sessuali da discutere con l’urologo.
Radiation e hormone: indicazioni
La radiotherapy esterna è impiegata sia come trattamento primario sia in associazione alla therapy ormonale (hormone therapy) nei tumori di rischio intermedio-alto. L’androgen deprivation therapy (ADT) riduce i livelli di testosterone e può essere combinata con radiation per migliorare il controllo locale e la sopravvivenza in determinate categorie. Gli effetti collaterali dell’hormone therapy richiedono monitoraggio: cambiamenti metabolici, perdita di massa muscolare e impatto sulla qualità di vita. La decisione su durata e intensità dell’ADT viene basata su parametri clinici e preferenze condivise.
Terapie sistemiche: chemotherapy e immunotherapy
Nei casi avanzati o metastatici, le opzioni sistemiche comprendono chemotherapy, farmaci ormonali di nuova generazione e immunotherapy in contesti selezionati. La chemotherapy può essere indicata per il carcinoma prostatico resistente alla castrazione o in presenza di burden metastatico significativo. L’immunotherapy è un campo in crescita: alcuni approcci sono approvati per sottogruppi specifici e altri sono esplorati in clinicaltrials. La valutazione di genetics e biomarkers orienta l’uso di terapie mirate e l’inclusione in studi sperimentali, migliorando la personalizzazione della terapia.
Genetics, biomarkers e clinicaltrials
Test genetici ereditari e somatici, insieme ai biomarker molecolari, stanno cambiando il paradigma decisionale: alcune alterazioni genetiche indicano maggior rischio di progressione e possono suggerire terapie mirate. La ricerca clinica (clinicaltrials) offre accesso a nuovi farmaci e combinazioni terapeutiche, particolarmente rilevante per pazienti con malattia avanzata o resistente. La sorveglianza (surveillance) post-trattamento utilizza PSA, imaging e, quando utile, test molecolari per identificare recidive o metastasis in fase trattabile. È consigliabile discutere l’opportunità di partecipare a studi clinici con il team sanitario.
Conclusione Le opzioni terapeutiche per la salute della prostata sono molteplici e in evoluzione: dalla sorveglianza attiva alle terapie locali e sistemiche, fino all’integrazione di dati genetici e biomarcatori per decisioni più mirate. La collaborazione multidisciplinare tra urology e oncology, supportata da imaging accurato e test diagnostici, consente di personalizzare il percorso terapeutico in base allo stadio della malattia e alle caratteristiche del paziente. Le scelte dovrebbero essere basate su evidenze, linee guida aggiornate e discussione informata con specialisti competenti.